FSMA - SOLICITUD
Ley de Modernización de la Seguridad Alimentaria de la FDA Resumen: Bajo el reconocimiento de la FDA, IAS tiene la autoridad para acreditar organismos de certificación de terceros, también conocidos como auditores de terceros.

FSMA - SOLICITUD
Ley de Modernización de la Seguridad Alimentaria de la FDA
Resumen: Bajo el reconocimiento de la FDA, IAS tiene la autoridad para acreditar organismos de certificación de terceros, también conocidos como auditores de terceros. Best ISO Certification Co. Ltd (Best ISO) es el organismo piloto de certificación que, una vez acreditado, puede realizar auditorías de seguridad alimentaria y emitir certificaciones de instalaciones alimentarias extranjeras (incluyendo granjas) y los alimentos -tanto humanos como animales- que producen. Esas certificaciones pueden ser utilizadas por los importadores para establecer la elegibilidad para participar en el Programa Voluntario de Importadores Calificados (VQIP), y en ciertas circunstancias la FDA puede requerir que los productos importados sean certificados antes de entrar en los Estados Unidos.
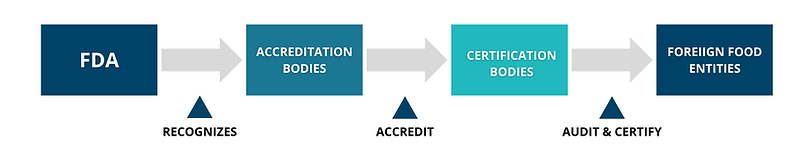
Introducción para FDA FSMA y VQIP
Este documento establece los requisitos para obtener y mantener el Servicio de Acreditación Internacional, Inc. (IAS), Organismos de Certificación de Terceros (Certificación Best-ISO) bajo la Ley de Modernización de Seguridad Alimentaria (FSMA) de la Administración de Alimentos y Medicamentos (FDA) y para los datos calificativos que deben presentarse en relación con el alcance de la Certificación. Los clientes de Certificación de Terceros que busquen acreditación para este programa de acreditación deberán cumplir con los requisitos especificados en el Registro Federal Vol.80, No. 228, de fecha 27 de noviembre de 2015, por la FDA; y complementado por este requisito del programa IAS, Reglas de Procedimiento de IAS para Organismos de Certificación de Terceros bajo la Ley de Modernización de Seguridad Alimentaria (FSMA) de la Administración de Alimentos y Medicamentos (FDA),
El Programa Voluntario de Importadores Calificados (VQIP) es un programa voluntario basado en tarifas que proporciona una revisión acelerada y la entrada de importaciones de alimentos para humanos y animales en los Estados Unidos para los importadores participantes. Tanto los consumidores como los importadores se beneficiarán de este programa.
Los importadores participantes podrán importar sus productos a los EE. UU. con mayor rapidez y previsibilidad, evitando demoras inesperadas en el punto de entrada de la importación. Los consumidores también se beneficiarán de la sólida gestión del importador de la seguridad y protección de sus cadenas de suministro.
Para participar, los importadores deben cumplir con los criterios de elegibilidad y pagar una tarifa de usuario que cubra los costos asociados con la administración del programa por parte de la FDA.
La Administración de Drogas y Alimentos de los EE. UU. (FDA) abrirá el portal de solicitudes del Programa de importadores calificados voluntarios (VQIP) el 1 de octubre de 2018. Esto permitirá a los importadores enviar sus solicitudes completas antes del año fiscal 2020. Los importadores interesados en presentar una solicitud pueden iniciar su solicitud enviando un aviso de intención de participar configurando una cuenta a través del sitio web de FDA Industry Systems . Una vez que tenga una cuenta, si selecciona VQIP en las opciones del programa FSMA, accederá a la página de solicitud de VQIP con una opción para enviar un Aviso de intención de participar. Los importadores que soliciten el período de beneficios del año fiscal 20 pueden consultar la guía paso a paso mientras preparan sus solicitudes.
Las tarifas anuales de usuario para participar en VQIP cubren los costos de la FDA para administrar el programa. Estos incluyen los costos de revisión de solicitudes; los costos de realizar inspecciones de los importadores (tanto extranjeros como nacionales) aceptados en el programa; y los costos anuales de mantenimiento de Tecnología de la Información (TI). Las tarifas de los usuarios se calculan cada año fiscal y se publicarán en un aviso del Registro Federal el 1 de agosto de cada año o antes.
Estas certificaciones se utilizan para dos propósitos.
- Las certificaciones pueden establecer la elegibilidad para participar en el Programa de Importadores Calificados Voluntarios (VQIP), que ofrece revisión e ingreso acelerados de alimentos.
- En circunstancias raras y específicas, la FDA puede exigir que un producto importado esté certificado para evitar que un alimento potencialmente dañino ingrese a los EE. UU.
El objetivo de alimentos importados de la Agencia es doble:
- Para abordar posibles problemas de seguridad antes de que los alimentos lleguen a los Estados Unidos; y
- Para ayudar a garantizar que los alimentos importados se produzcan de acuerdo con los mismos estándares de seguridad que se exigen a los alimentos estadounidenses.
Los organismos de acreditación bajo el Programa de Certificación de Terceros Acreditados deben:
- Evalúe los organismos de certificación de terceros para determinar si pueden ser acreditados. Esto incluye observar una muestra representativa del trabajo del solicitante;
- Supervisar el desempeño de los organismos de certificación que acredita. Los organismos de acreditación deben notificar a la FDA sobre cualquier cambio o retiro de las acreditaciones que haya otorgado;
- Evaluar y corregir cualquier problema en el propio desempeño del organismo de acreditación;
- Presentar informes de seguimiento y autoevaluación y otras notificaciones a la FDA;
- Mantener y proporcionar acceso a la FDA a los registros que requiere el programa.
El Programa de Certificación de Terceros Acreditados de la FDA se estableció en virtud de la Ley de Modernización de la Seguridad Alimentaria (FSMA) de la FDA. Es un programa voluntario que permite que los "organismos de acreditación" soliciten el reconocimiento de la FDA. Los organismos de acreditación reconocidos tendrán la autoridad para acreditar organismos de certificación de terceros.
Solicitud
1.0 Todos los clientes deben entregar la siguiente información de la solicitud antes de la programación de la auditoría.
- Contrato
- Formulario de solicitud (Adjunto A formulario 1)
- Cuestionario para FDA (Adjunto B- Formulario 2-8)
- Plan de seguridad alimentaria emitido por persona calificada PCQI
- FSMA - Manual de calidad (no requisito)
- Evidencia de conformidad con los requisitos de seguridad alimentaria aplicables de la Ley FD&C y las regulaciones de la FDA
- Información relativa anterior de la FDA
2.0 Y comprender los siguientes requisitos para el requisito especial BEST ISO-IAS-FDA FSMA.
- Toda la auditoría debe realizarse sin previo aviso durante el plazo de 30 días identificado.
- La auditoría de preparación ST1 para verificar el sistema y que todo el día hombre mínimo sea un día hombre debe centrarse en determinar si la instalación, sus procesos y los alimentos cumplen con los requisitos de seguridad alimentaria aplicables de la Ley FD&C y la FDA. reglamento, (adjunto C)
- ST2 seguirá el formulario de día de trabajo (adjunto D) para una auditoría in situ para (NIC 4.10.2) el examen de la instalación, su(s) proceso(s) y los alimentos que resultan de dicho(s) proceso(s); y cuando corresponda o cuando requerido por FDA, muestreo y análisis ambiental o de productos. Cuando, para una auditoría reglamentaria, se realice un muestreo y análisis, el organismo de certificación de terceros acreditado debe utilizar un laboratorio que esté acreditado de conformidad con el párrafo 1.8 de este documento. arriba. La auditoría puede incluir cualquier otra actividad necesaria para determinar el cumplimiento de los requisitos de seguridad alimentaria aplicables de la Ley FD&C y las reglamentaciones de la FDA y, en el caso de las auditorías consultivas, también incluye el cumplimiento de las normas y prácticas aplicables de la industria. (1.12)ISO9001 con HACCP o ISO22000 (IAS-4.10.3.
3.0 BEST ISO tiene un acuerdo legalmente exigible para la provisión de actividades de certificación a su cliente.
Este acuerdo legalmente exigible incluye disposiciones para garantizar que pueda extenderse hasta que se completen todas las actividades de transferencia al nuevo organismo de certificación reconocido por la FDA.
El contrato entre el organismo de certificación y el cliente deberá abordar los siguientes elementos:
a) el cliente deberá notificar al organismo de certificación de cualquier cambio (ver sección 3.2),
b) el cliente no puede rechazar una auditoría de testigo FDA e IAS del organismo de certificación,
c) el cliente no puede rechazar la presencia de un auditor testigo interno del organismo de certificación,
d) el cliente no puede rechazar la presencia de un representante de FDA & IAS o sus delegados,
e) el cliente no puede rechazar la solicitud del organismo de certificación de proporcionar el informe final a FDA e IAS,
f) el único uso del logotipo FDA e IAS relacionado con este esquema de certificación es el que se muestra en el certificado emitido por el organismo de certificación. Queda prohibido cualquier otro uso del logotipo FDA e IAS, por separado o no.
g) los consultores del cliente no pueden estar físicamente presentes en el sitio del cliente durante la auditoría ni participar en la auditoría de ninguna manera
h) el cliente deberá pagar todos los honorarios por adelantado y que no habrá devolución alguna.
i) La certificación tiene una vigencia máxima de 12 meses a partir del día de su emisión. Ciclo del certificado: La decisión de recertificación se tomará antes de la fecha de vencimiento del certificado existente. La fecha de la decisión de recertificación será la fecha de emisión del nuevo certificado.
J) El informe de auditoría en inglés debe entregarse a IAS y FDA
Revisión de documentos
Formulario de solicitud de contrato
Cuestionario-EH1 para FDA (Adjunto B- Formulario 2-8)
Plan de seguridad alimentaria emitido por persona calificada PCQIFSMA - Manual de calidad (No requisito)
Evidencia de conformidad con los requisitos de seguridad alimentaria aplicables de la Ley FD&C y las regulaciones de la FDA
Información relativa anterior de la FDA
BEST ISO GROUP
Best ISO Group
Chimalhuacán 3569 Piso 8,
Cd del Sol, 45050 Zapopan, Jal.
México.
Horario:
Lunes a Viernes 9:00 am - 5:00 pm
Avisos Legales
Contacto
Correo: info@bestisogroup.com
Teléfono: +52 333 121 2445
